Vanda solicita autorización para Imsidolimab en psoriasis pustulosa generalizada
**Introducción**
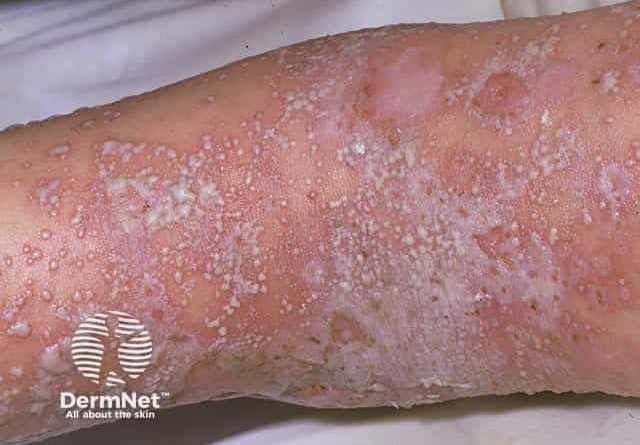
La psoriasis pustulosa generalizada (GPP) representa una de las formas más complejas y potencialmente graves de psoriasis, caracterizada por brotes agudos con pústulas estériles sobre áreas eritematosas de la piel. Se trata de una condición rara, con un manejo clínico desafiante para los profesionales de la estética avanzada y la medicina estética, dada su presentación impredecible y la limitada eficacia de los tratamientos convencionales. En este contexto, la reciente solicitud de autorización de comercialización (Biologics License Application, BLA) por parte de Vanda Pharmaceuticals para imsidolimab, un anticuerpo monoclonal dirigido contra el receptor de interleucina-36 (IL-36R), supone un avance relevante para el abordaje de la GPP desde la perspectiva de la estética avanzada y la dermatología clínica.
**Novedad o Tratamiento**
Imsidolimab es un anticuerpo monoclonal humanizado de tipo IgG4 que actúa inhibiendo la señalización de IL-36R, una vía implicada directamente en la patogénesis de la psoriasis pustulosa generalizada. El fármaco se administra por vía intravenosa y está diseñado para controlar los brotes agudos de GPP, reduciendo la inflamación y las lesiones pustulosas de manera más eficaz y rápida que las terapias sistémicas tradicionales.
**Características Técnicas**
El principio activo, imsidolimab, se produce mediante tecnologías recombinantes avanzadas y presenta una elevada afinidad por el receptor IL-36R, bloqueando la cascada inflamatoria mediada por las interleucinas IL-36α, IL-36β e IL-36γ. Su vida media se sitúa en torno a las dos semanas, permitiendo una pauta de administración espaciada (habitualmente, una infusión inicial seguida de dosis de mantenimiento mensuales). El anticuerpo se presenta en viales liofilizados para reconstitución y administración intravenosa en entornos clínicos especializados.
**Innovaciones respecto a modelos anteriores**
Mientras que los tratamientos sistémicos tradicionales para GPP incluyen retinoides orales, metotrexato, ciclosporina y corticoides, así como biológicos anti-TNF y anti-IL-17, la diana terapéutica de imsidolimab es específica y novedosa. Hasta la fecha, sólo spesolimab (otro anti-IL-36R, de Boehringer Ingelheim) había sido aprobado para GPP, lo que sitúa a imsidolimab como una alternativa con potenciales ventajas en perfil de seguridad, eficacia y posología. La especificidad de la inhibición de IL-36R reduce la inmunosupresión sistémica global y, por tanto, el riesgo de infecciones oportunistas.
**Evidencia y Estudios recientes**
El programa de desarrollo clínico de imsidolimab incluye el estudio pivotal de fase III, “Effisayil 2”, cuyos resultados preliminares fueron publicados en 2023. Dicho estudio demostró que una única infusión de imsidolimab logró una resolución rápida y sostenida de los brotes agudos de GPP en una proporción significativa de pacientes, con un perfil de eventos adversos comparable al placebo (Kimball AB et al., 2023). Además, el control de la inflamación y la reducción del dolor y el malestar asociados a las lesiones resultaron en mejoras objetivas de la calidad de vida.
**Ventajas y Limitaciones**
Las principales ventajas de imsidolimab radican en su acción selectiva sobre la vía IL-36, la rapidez de respuesta observada en los brotes agudos y la posibilidad de reducir la carga global de inmunosupresión. Para los profesionales de la estética avanzada que trabajan en coordinación con dermatólogos, este tipo de biológicos abre nuevas vías de intervención para el manejo de la GPP y el control de sus secuelas estéticas, tales como hiperpigmentaciones postinflamatorias o cicatrices residuales.
Sin embargo, como limitación principal se señala el coste de los anticuerpos monoclonales (estimado entre 7.000 y 10.000 euros por ciclo de tratamiento), así como la necesidad de administración hospitalaria o en clínicas con infraestructura para infusión intravenosa y monitorización. No está indicado para otras formas de psoriasis ni para el mantenimiento a largo plazo fuera de los brotes agudos.
**Opinión de Expertos**
Dermatólogos y especialistas en medicina estética coinciden en que la llegada de imsidolimab representa un avance relevante en el arsenal terapéutico para la GPP, especialmente en pacientes refractarios o intolerantes a terapias previas. Según la Dra. A. Sánchez, dermatóloga experta en biológicos, “la inhibición dirigida de IL-36R permite un control mucho más preciso de la inflamación, lo que reduce las complicaciones y mejora la calidad de vida del paciente en comparación con los inmunosupresores clásicos”.
**Aplicaciones prácticas en centros y clínicas de estética y medicina estética**
En el entorno de la estética avanzada y la medicina estética, la disponibilidad de imsidolimab permitirá una colaboración más estrecha con dermatología para el abordaje multidisciplinar de pacientes con GPP. Los centros que ofrezcan tratamientos complementarios para las secuelas estéticas de la GPP (láser no ablativo, radiofrecuencia fraccionada, microagulllamiento con principios activos despigmentantes como ácido tranexámico, etc.) podrán integrar de forma segura estos procedimientos una vez controlados los brotes agudos con imsidolimab, optimizando los resultados estéticos y la satisfacción del paciente.
**Conclusiones**
La solicitud de autorización de imsidolimab por parte de Vanda Pharmaceuticals supone un avance relevante en el tratamiento de la psoriasis pustulosa generalizada. Su mecanismo de acción específico y su eficacia demostrada en estudios recientes posicionan a este anticuerpo como una herramienta innovadora, que permitirá a los profesionales del sector estético ofrecer mejores soluciones integrales, colaborando con dermatología para el manejo tanto de la enfermedad activa como de sus secuelas estéticas.
(Fuente: www.dermatologytimes.com)