Veradermics inicia ensayo fase 2/3 de VDPHL01, primer tratamiento oral para alopecia femenina
Introducción
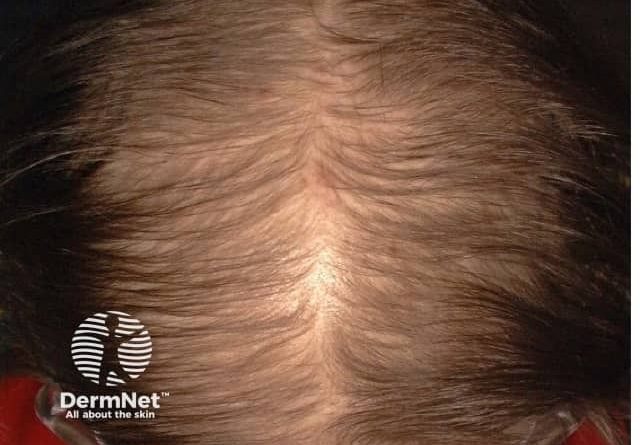
La alopecia androgenética femenina, conocida como FPHL (Female Pattern Hair Loss), representa uno de los desafíos más relevantes en la consulta de medicina estética y dermatología capilar avanzada. El interés creciente de la población femenina en soluciones efectivas y seguras ha impulsado la investigación de nuevas alternativas terapéuticas. En este contexto, la compañía estadounidense Veradermics ha anunciado el inicio de un ensayo clínico fase 2/3 para su innovador fármaco oral VDPHL01, que podría convertirse en el primer tratamiento oral aprobado por la FDA específicamente para la alopecia androgenética femenina. Este desarrollo supone un avance potencialmente disruptivo para clínicas médico-estéticas, centros capilares y consultorios privados especializados en tricología.
Novedad o Tratamiento
El VDPHL01 es un fármaco de administración oral orientado al tratamiento específico de la FPHL. A diferencia de los tratamientos tópicos tradicionales como el minoxidil o las soluciones combinadas con finasterida (mayoritariamente aprobadas para varones), el VDPHL01 se posiciona como una alternativa oral diseñada y testada exclusivamente para mujeres. Este enfoque responde a una demanda creciente en el sector estético y médico-estético, donde la adherencia y la comodidad del paciente son factores clave para el éxito de los protocolos.
Características Técnicas
Aunque los detalles concretos sobre la composición molecular de VDPHL01 permanecen bajo confidencialidad industrial, las primeras informaciones apuntan a que se trata de un modulador selectivo de los receptores hormonales implicados en la miniaturización folicular característica de la FPHL. El objetivo es actuar directamente sobre la etiopatogenia de la alopecia androgenética femenina, evitando los efectos adversos asociados a los inhibidores de la 5-alfa reductasa empleados en varones (como la finasterida o dutasterida) y a los antiandrógenos clásicos como la espironolactona, que presentan limitaciones de seguridad y eficacia.
La administración oral, prevista en una posología diaria, busca mejorar la adherencia y reducir la variabilidad de resultados asociada a la aplicación tópica. Se prevé que el fármaco se presente en comprimidos de fácil deglución, optimizados para una liberación controlada y una biodisponibilidad adecuada en el tejido folicular.
Innovaciones respecto a modelos anteriores
El lanzamiento del estudio de fase 2/3 supone una innovación en varios frentes. En primer lugar, es el primer desarrollo de un tratamiento oral encaminado a obtener la aprobación específica de la FDA para la alopecia femenina, un segmento tradicionalmente infraatendido. Hasta el momento, la mayoría de los tratamientos orales utilizados (como finasterida o dutasterida) son off-label y con indicaciones aprobadas solo para varones.
El VDPHL01 introduce un perfil de seguridad teóricamente superior, minimizando riesgos de teratogenicidad y efectos secundarios hormonales, uno de los principales escollos en el tratamiento oral de la FPHL. Además, la molécula estaría diseñada para evitar la interacción con anticonceptivos orales y no requeriría monitorización hormonal exhaustiva, facilitando su integración en los protocolos de las clínicas estéticas.
Evidencia y Estudios recientes
El ensayo fase 2/3 anunciado por Veradermics implica la inclusión de un número significativo de pacientes (se estima entre 200 y 400 mujeres adultas diagnosticadas de FPHL) y se desarrollará en centros especializados de Estados Unidos y Europa. Los principales criterios de valoración incluirán el recuento de cabellos terminales, la densidad capilar medida por tricoscopía digital y la autoevaluación de los pacientes.
Aunque los resultados oficiales de la fase 2/3 no estarán disponibles antes de 2025, estudios previos de fase 1 (Veradermics, 2023) han mostrado una tolerabilidad excelente y una tendencia positiva en la reducción de la caída y el aumento de densidad capilar en un periodo de 24 semanas.
Ventajas y Limitaciones
Entre las ventajas principales, destaca la vía de administración oral, la potencial ausencia de efectos virilizantes o alteraciones hormonales significativas, y la posibilidad de prescribir el tratamiento a un segmento amplio de mujeres, incluidas aquellas en edad fértil bajo anticoncepción. En comparación con minoxidil tópico (tratamiento de referencia según guías NICE 2022), el VDPHL01 podría mejorar la adherencia y la satisfacción del paciente, aspectos críticos en la práctica profesional.
Como limitaciones, el fármaco se encuentra aún en investigación clínica, por lo que no está disponible en el mercado ni autorizado para su uso fuera de ensayos. El coste estimado, una vez aprobado, podría situarse en torno a los 200-300 € mensuales, similar a las terapias de última generación en tricología avanzada.
Opinión de Expertos
Según la Dra. Marta García, especialista en medicina capilar y directora de una clínica de referencia en Madrid, “el desarrollo de una molécula oral específica para FPHL responde a una necesidad no cubierta en el sector. Si se confirman los datos de eficacia y seguridad, supondrá un cambio de paradigma en el abordaje médico-estético de la alopecia femenina”.
Aplicaciones prácticas en centros y clínicas de estética y medicina estética
De confirmarse su aprobación, el VDPHL01 permitirá a los profesionales de la estética avanzada y la medicina estética incorporar un nuevo protocolo oral a sus tratamientos capilares. Podría emplearse como monoterapia o en combinación con otros procedimientos como mesoterapia capilar (Dutasterida, vitaminas, péptidos biomiméticos), tecnologías de bioestimulación (Láser de baja potencia, LLLT), y dispositivos de microagujas (Dermapen). La facilidad de administración y el perfil de seguridad lo harían especialmente atractivo para consultas privadas y clínicas con alto volumen de pacientes femeninas.
Conclusiones
El inicio del ensayo fase 2/3 de VDPHL01 marca un hito en la innovación terapéutica para la alopecia androgenética femenina. Su potencial como primer tratamiento oral aprobado para FPHL podría redefinir los protocolos en centros de estética avanzada y clínicas médico-estéticas, aumentando la oferta de soluciones eficaces, seguras y cómodas para la paciente femenina actual. Se recomienda a los profesionales del sector mantenerse actualizados sobre la evolución de este desarrollo y valorar su futura integración en la práctica clínica.
(Fuente: www.dermatologytimes.com)